
Allt om nedfrysning, lite om flytande kväve och hemmagjord Solero
Att nedfrysning är en komplex process blir tydligt när man försöker beräkna exakt hur lång tid det tar för ett ämne att frysa. All vår föda innehåller vatten i någon form och därför är vatten den i särklass viktigaste faktorn i då vi talar om nedfrysning av livsmedel.
(Skulle du få för dig att räkna ut exakt hur lång tid det tar att frysa ner någonting så är det Pham’s equation du ska använda).
Dessa invecklade beräkningar kanske inte behövs varje gång du skall öppna dörren till frysen, men det finns några aspekter som man bör tänka på. När mat skall frysas är huvudanledningen oftast att förlänga hållbarheten. Då vill man gärna minimera frysskador och kanske även ta reda på hur man på bästa sätt tinar upp maten*. Vissa vill dessutom veta hur man minimerar formationen av iskristaller i mat, framförallt i glass. Det kan man styra med hjälp av ingredienser som socker, alkohol, ice cream stabilizer eller fruktkärnmjöl. Även om dosering av dessa tillsatser är perfekt men tillsatserna fryses ner för långsamt, och/eller utan tillräcklig omrörning, kommer oönskade iskristaller ändå att bildas. Nedfrysningstiden är därför den enskilt viktigaste faktorn för storleken på iskristallerna i glass.
*(notera att upptining inte är motsatsen till frysning, men det tar vi i en annan artikel)
Iskristaller och kristallbildning
Vad händer när vi fryser någonting? En grundläggande insikt som behövs för att förstå dessa processer är att nedkylning inte egentligen är tillförsel av kyla. Kyla är nämligen bara avsaknad av värmeenergi (precis som mörker endast är frånvaro av ljus). När vi säger att vatten fryser är det egentligen ett byte av aggregationstillstånd, nämligen omvandling från vätska till kristallin form vi talar om. Detta sker när substansen tappat så mycket värmeenergi som behövs för att detta - energifattigare - tillstånd skall uppstå. För att denna kristallformation ska ske måste det ske en nukleation av vattenmolekyler, d v s kärnbildning av en ny termodynamisk fas av vatten. Det är inte så komplicerat som det låter, is måste börja bildas någonstans och kärnbildningen är det första händelseförloppet när iskristaller bildas.
Nukleation sker huvudsakligen på två sätt. Antingen genom en så kallad homogen kärnbildning, vilket betyder att vattenmolekylerna i princip slumpmässigt kommer att bilda en nukleationspunkt, eller kärna, på någon plats. Detta är högst osannolikt i ett normalt kök då maten måste bli mer än “underkyld” på en väldigt kort tid för att kristallisering på detta sätt ska ske. Det är dock inte helt omöjligt och jag kommer att återkomma till det lite längre ner. Det vanligaste är istället att maten går igenom en så kallad heterogen kärnbildning, där nedkylningen bildar mer regelmässiga punkter runt cellväggar eller andra partiklar där de kan ta fäste.
I den heterogena kärnbildningen går det att påverka hur många punkter som ska bildas. Är det färre nukleationspunkter blir kristallerna större och är det många punkter blir kristallerna mindre. Detta hänger ihop med hur snabb nedkylningen är. En långsam nedfrysning ger få och stora iskristaller, vilket inte önskas. Detta kan även påverka strukturen i till exempel grönsaker då de stora kristallerna kan spränga cellerna och därmed förstöra råvarans struktur. Det påverkar även strukturen i glass som kommer fortsättas att användas som ett exempel nedan.
En snabb nedfrysning ger många och små kristaller vilket är precis det som önskas.
Lite teoretiska aspekter i nedfrysningsprocessen
Så i grund och botten, iskristaller i glass beror på en mängd olika faktorer, men utan en tillräckligt snabb nedfrysning så kommer det att bildas för stora iskristaller.
Om nedfrysningen sker på rätt sätt så kommer det se ut ungefär som figuren nedan.
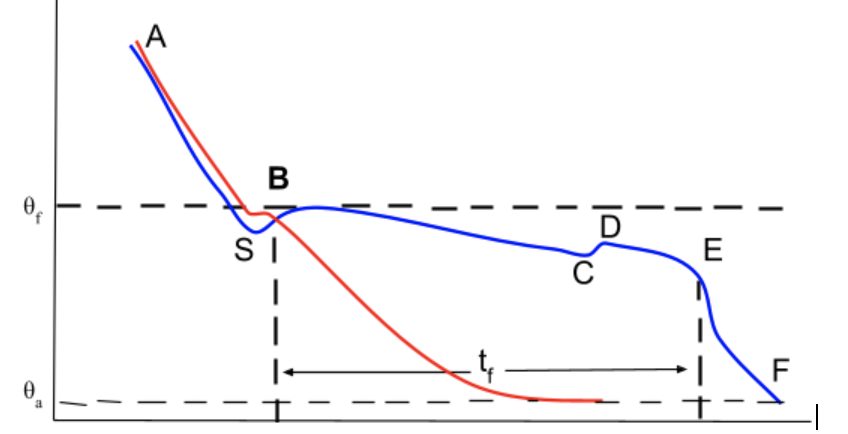
Den streckade linjen i mitten är 0 grader, fryspunkten för vatten. Den blå linjen motsvarar nedfrysning av ett “vanligt” livsmedel. Den röda linjen motsvarar ett livsmedel med exempelvis mycket högre sockerhalt, vilket kan vara glass med mer eller mindre socker.
Från punkt A till punkt S kyls vattnet ner till under sin fryspunkt. Vid punkten S är vattnet fortfarande i flytande form, även fast det är under 0 grader. Det här kallas underkylning och det är här vattnet först börjar att kristalliseras.
Från S till B börjar iskristaller att formas, vilket leder till ett energiutsläpp, alltså att den latenta värmen släpps ut. Detta medför att temperaturen går upp, därav den lilla uppgången i kurvan. Det är därför det går så långsamt för något att kylas ner mellan punkt B och C vilket är därför detta är ett kritiskt moment i nedkylningsprocessen. Av den anledningen är det viktigt att detta steg ska gå så fort som möjligt så att inte för stora iskristaller bildas.
Som den röda kurvan med högre sockerhalt visar, får sockret ner fryspunkten och det sker en snabbare nedkylning vilket leder till att det bildas mer små iskristaller. Sockret minimerar även mängden fritt vatten som kan bilda kristaller vilket ytterligare bidrar till en bättre kristallformation.
I glasstillverkning kan denna platå mellan B och C styras genom att man rör om i glassen så att kylan distribueras bättre. Det är dock inte bara därför man rör om i en glassmet, mer om detta kan läsas i Jonas text om hemmagjord gelato och glass
Denna frysplatå (tf) uppstår eftersom smeten slutar att bli kallare så länge det finns frysbart vatten som inte har kristalliserat, och medan det händer så behöver värme frigöras. När mer is formas kommer temperaturen successivt att gå ner.
Om du inte har slutat läsa än, så kanske följande punkter kommer få dig att göra det, men de är ytterst viktiga om vi ska förstå vad som faktiskt händer i frysen och hur det påverkar, exempelvis glass.
Mellan punkt C och D går temperaturen upp. Det här är den eutektiska punkten, då diverse ämnen i det som fryser inte längre klarar av att vara lösligt i den kalla temperaturen och kristalliseras ut. Enklast är att jämföra det med när vi fryser saltvatten. Detta görs för att få ner temperaturen på vattnet så att det kan bli kallare än vanlig is. När saltvattnet når -20oC, kommer vattnet att bli mättat på salt vilket leder till att saltet då kommer att kristalliseras ut och vattnet fryser. I glass kommer laktosen, som är väldigt olöslig i kalla temperaturer, att kristalliseras ut. Vad detta har för betydelse kommer det mer om längre fram.
Efter detta kommer all vätska att kristalliseras och temperaturen kommer att sjunka till den temperatur frysen är inställd på.
Re-kristallisering och glastransitionstemperatur
Nu tänker du såklart att, men hallå! Temperaturen fortsätter ju att sjunka i den där lilla figuren, och nu undrar du varför jag har ritat dit linjen mellan E till F… Det är faktiskt nu som saker börjar att bli lite mer intressanta. Eller så är det jag som inte vet när jag ska sluta skriva.
Om vi kan få ner temperaturen ytterligare, så kommer det vi fryser att sjunka till den så kallade “glastransitionstemperaturen”. Väldigt enkelt förklarat, så kommer den att ändra stat inom fasen. Det kanske fortfarande var lite för oklart. Mer enkelt förklarat: en spagetti är solid och befinner sig i ett glasstadie när den är okokt. När den kokas så är den fortfarande solid, men då den går över i ett så kallad läderstadie. Den går då genom en glastransition.
Varför är det här viktigt? Jo, om vi nu har gjort vår glass och lägger den i frysen så kommer glassen att smälta och frysa igen. Detta sker på grund av att glassen fortfarande är väldigt instabil och att det sker flera väldigt små temperaturskillnader, vilket händer även i de bästa frysar. När glassen smälter och fryser igen kommer det att bildas fler och större iskristaller i glassen, dessutom kommer fettet i glassen att separera från emulsionen och kristalliseras. Vidare så är laktos, som nämndes tidigare, väldigt olösligt i dessa temperaturer och vill gärna kristalliseras ut från lösningen den befinner sig i. Detta kan göra att glassen blir isig och sandig i konsistensen.
För att motverka att detta händer så måste vi därför få ner glassen till under sin glastransitionstemperatur, där den inte är lika instabil och reaktiv längre, så att den får längre hållbarhet och fortsätta att vara krämig och god. Det är bara det lilla problemet att glastransitionstemperaturen för glass ligger runt -40oC.
Så vad ska göras nu då? För att få en bra glass måste den frysas snabbt för att minimera storleken på iskristallerna. Mängden fritt vatten måste också minskas för att minimera kristallisering. Vidare måste fryspunkten sänkas, vilket kan ge en snabbare nedfrysning. Dessutom måste glastransitionstemperaturen höjas för att glassen ska vara stabil i frysen och inte råka ut för rekristallisering samt att laktoset måste förhindras från att kristalliseras ut från glassen.
Det är faktiskt precis därför det finns ingredienser som till exempel, Locust bean gum (fruktkärnmjöl), Xanthan gum, Guar Gum och Metylcellulosa. Alla dessa har lite olika funktioner och används väldigt ofta tillsammans i blandningar som Ice cream stabilizer.
Flytande kväve (N2(l))
Tidigare i texten nämns homogen kärnbildning och att få ner temperaturen så snabbt så att alla dessa problem undviks. Detta kan enkelt uppnås med hjälp av flytande kväve.
Flytande kväve är, som det låter, kväve i flytande form. För att få ner den i denna fas så måste den kylas ner till -195.8° C. Med hjälp av extrem kyla går det att få till en riktigt krämig glass, snabbt och dessutom behövs det inte en glassmaskin utan bara en vanlig matberedare. Kanske är det enklare att köpa en glassmaskin än att få tag på flytande kväve. Hur som helst, har vi ett provkök (läs lekstuga) på KitchenLab, där det finns en hel tank med flytande kväve som öppnar upp möjligheten för lite nya kreationer.
Det finns recept som kräver flytande kväve för att de ens ska kunna tillverkas. Ett av dessa är de små glasskulorna, eller glasshotsen vi åt för kanske 20 år sedan. För att detta ens ska vara görbart och kunna formas till små kulor måste glassmeten därför droppas ner i flytande kväve så att den fryser direkt.
Till detta går det att använda en vanlig glassmet, men traditionellt görs det på Sherbert som är lite som en sorbet fast med mjölk eller grädde i. Vi testade såklart att göra detta. Resultatet ser du i videon nedan.
